Chapitres
Remarque préalable : Il est difficile, à notre niveau, de traiter ce chapitre de façon uniquement théorique et abstraite. Le parti pris ici est de développer les connaissances à partir d'un exemple. Il appartient à chacun d'assimiler les notions présentées à partir de cet exemple de façon à pouvoir les utiliser dans d'autres cas.


Les transformations chimiques
Exemple
Le dihydrogène peut réagir de façon explosive avec le dioxygène pour donner de l'eau. Nous supposerons qu'il reste du dioxygène à la fin de la transformation.
Système et transformation chimique
Le système chimique est constitué par l'ensemble des espèces chimiques auxquelles on s'intéresse.
L'état d'un système chimique est caractérisé par :
- Les grandeurs physiques P (pression du ou des gaz) et T (température),
- L'état physique, liquide (l), solide (s), gazeux (g) et aqueux (aq) des espèces présentes,
- Les quantités de matière des espèces présentes.
On prendra l'habitude de représenter l'état d'un système comme il est indiqué ci-contre :

La transformation chimique est le passage du système de l'état initial à l'état final (voir ci-contre).
Le réactif limitant (ou réactif en défaut) est le réactif totalement consommé par la réaction. Il n'en reste plus à la fin de la réaction. C'est le cas du dihydrogène ici.
La réaction chimique et son équation

La réaction chimique
La réaction chimique modélise la transformation chimique subie par un système.
L'équation (ou équation-bilan) d'une réaction
L'équation d'une réaction est l'écriture symbolique d'une réaction chimique. Elle comporte :
- Une flèche qui indique le sens de la transformation,
- A gauche de la flèche, les symboles des réactifs séparés par des signes +,
- A droite de la flèche, les symboles des produits de la transformation séparés par des signes +.
- Des nombres stœchiométriques, placés devant chaque symbole, choisis de telle façon que la loi de conservation des éléments soit satisfaite. On dit qu'on ajuste les nombres stœchiométriques.
Remarques
- Le nombre stœchiométrique 1 n'est jamais écrit.
- Si la transformation met en jeu des ions, l'ajustement des nombres stœchiométriques doit aussi réaliser la conservation de la charge électrique.
Exemple

ou 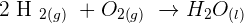
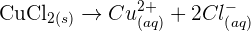
Équation et quantité de matière
Les nombres stœchiométriques indiquent dans quelles proportions les quantités de matières des réactifs réagissent et ce quelques soient les quantités de matières des réactifs mis en présence. Par exemple l'équation de la réaction de formation de l'eau donnée en 3 indique que :
si x mol de O2 disparaissent alors 2x mol de H2 disparaissent aussi et il se forme 2x mol de H2O.
Avancement et bilan de matière
Avancement de la réaction
Considérons la réaction chimique dont l'équation est : aA + bB ![]() cC + dD où A et B sont les réactifs, C et D les produits et a, b, c et d sont les nombres stœchiométriques.
cC + dD où A et B sont les réactifs, C et D les produits et a, b, c et d sont les nombres stœchiométriques.
Les notations utilisées dans la suite sont résumées ci-dessous :
- x : avancement de la réaction ;
- n(A)0 : quantité de matière initiale de A ;
- n(A) : quantité de matière de A à la date t ;
- n(A)f : quantité de matière finale de A.
Voici un exemple de tableau d'avancement :
| Équation de la réaction | aA | + | bB | = | cC | + | dD |
|---|---|---|---|---|---|---|---|
| Etat initial (mol) | n(A)0 | + | n(B)0 | = | n(C)0=0 | + | n(D)0=0 |
| Etat à l'instant T (mol) | n(A)=n(A)0-axt | + | n(B)=n(B)0-bxt | = | n(C)=cxt | + | n(D)=dxt |
| Etat à la fin de la réaction (mol) | n(A)f=n(A)0-axf | + | n(B)f=n(B)0-bxf | = | n(C)f=cxf | + | n(D)f=dxf |
Il en est de même pour les autres espèces.
L'avancement final est un avancement qui est réellement observé, atteint. Mais l'avancement maximal correspond également à l'avancement atteint lorsqu'un réactif est entièrement consommé (avancement théorique observable).
En reprenant l'exemple précédent, x est appelé avancement de la réaction à la date t. Ce nombre permet de suivre l'évolution de la transformation et donc de caractériser le système à un moment donné.
L'avancement maximal xmax s'obtient en écrivant que les quantités de matières des réactifs sont toujours positives ou nulles.
Nous supposerons, cette année qu'une réaction s'arrête lorsqu'un des réactifs a été totalement consommé. Ce réactif est appelé réactif limitant. Il est tel que sa quantité de matière est nulle (il n'en reste plus) lorsque x = xmax, c'est-à-dire lorsque l'avancement est maximal.
Dans certains cas tous les réactifs sont totalement consommés. On dit alors qu'ils ont été introduits dans les proportions stœchiométriques.
Taux d'avancement τ
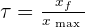
- Si τ ≤ 1 => si τ = 1 xf = xmax alors on est en présence d'une réaction totale
- τ < 1 , xf ≠ xmax alors on est en présence d'une réaction partielle qui s'arrête lorsqu'elle atteint l'équilibre chimique.
Relation entre l'avancement et la concentration molaire volumique
Si on ne prend en compte que le cas particulier d'une réaction ayant lieu en solution aqueuse telle que le volume V de la solution soit constant, alors on peut utiliser l'expression suivante :
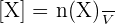
Avec :
- [X] représentant la concentration molaire (en mol.L-1) ;
- n(X) représentant la quantité de matière de l'espèce X en solution (en mol) ;
- V représentant le volume de la solution (en L).
D'après ce qui précède, en divisant tous les termes de la relation de définition de l'avancement par V :
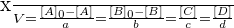
Vitesse volumique de réaction
Définition
On peut définir la vitesse volumique de réaction avec l'aide de l'expression suivante :
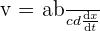
Avec :
- v représentant la vitesse volumique de réaction (en mol.m-3.s-1) ;
- V représentant le volume de la solution (en m3) ;
- dx représentant la variation de l'avancement (en mol) ;
- dt représentant la durée de la variation (en s).
Remarques :
- Il arrive fréquemment que le volume V soit exprimé en litre. La vitesse de réaction est alors exprimée en mol.L-1.s-1 ;
- Si la transformation est lente ou très lente la durée peut être exprimée en minute ou en heure. La vitesse de réaction est alors exprimée en mol.L-1.min-1 ou en mol.L-1.h-1 ;
- Le rapport dx/dt représente la dérivée par rapport au temps de l'avancement.
Bilan de matière
Rappelons que les quantités de matières peuvent être déterminées à partir des masses ou des volumes (plus particulièrement pour les gaz) en utilisant les relations suivantes déjà rencontrées :
 et
et 
Supposons que l'on réalise une réaction chimique en mettant en présence 0,2 mol de dioxygène et 0,2 mol de dihydrogène. Dressons un bilan complet de matière.
Ce bilan est, en général, présenté sous forme de tableau que l'on construit progressivement.
| Équation de la réaction |
| ||
|---|---|---|---|
| Quantité de matières initiales (mol) | n(H2)i =0,2 | n(O2)i =0,2 | n(H2O)i =0,0 |
| Quantités de matières de réactifs consommés et de produits formés à la date t (mol) | n(H2) = 2x | n(O2) = x | n(H2O) = 2x |
| Quantités de matières présentes à la date t (mol) lorsque l'avancement est x | n(H2)t = 0,2 - 2x | n(O2)t = 0,2 - x | n(H2O)t = 2x |
| Quantités de matières finales (mol) lorsque l'avancement est xmax | n(H2)f = 0,2 - 2 xmax | n(H2)f = 0,2 - xmax | n(H2O)f = 2 xmax |
A ce stade de l'étude, le tableau n'est pas complet car xmax n'est pas connu et reste à déterminer. Il est possible de déterminer xmax de deux manières différentes :
Méthode des quantités de matières toujours positives ou nulles
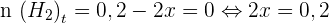
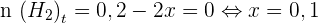

Les deux dernières inégalités sur x sont satisfaites pour x = 0,1. On retiendra donc la valeur xmax = 0,1 mol. Il devient alors possible de compléter la dernière ligne du tableau précédent.
| Équation de la réaction |
| ||
|---|---|---|---|
| Quantité de matières initiales (mol) | n(H2)i =0,2 | n(O2)i =0,2 | n(H2O)i =0,0 |
| Quantités de matières de réactifs consommés et de produits formés à la date t (mol) | n(H2) = 2x | n(O2) = x | n(H2O) = 2x |
| Quantités de matières présentes à la date t (mol) lorsque l'avancement est x | n(H2)t = 0,2 - 2x | n(O2)t = 0,2 - x | n(H2O)t = 2x |
| Quantités de matières finales (mol) lorsque l'avancement est xmax | n(H2)f = 0,0 | n(H2)f = 0,1 | n(H2O)f = 0,2 |
Le dihydrogène est totalement consommé il apparaît comme le réactif limitant.
Méthode graphique
On trace dans le même repère les droites d'équations :
n(H2)t = 0,2 - 2x et n(O2)t = 0,2 - x.
Lorsque x croît, c'est-à-dire lorsque la réaction évolue, sa valeur maximale xmax est atteinte lorsque la droite n(H2)t = 0,2 - 2x coupe l'axe des abscisses. On a alors xmax = 0,1 mol.
D'une façon plus générale, xmax s'obtient en considérant les intersections des droites du graphique avec l'axe des abscisses et en choisissant celle qui a l'abscisse la plus petite.
Les réactions à connaître
Les réactions d'oxydo-réduction

Une réaction d'oxydoréduction, également appelée réaction redox, correspond à une réaction chimique au cours de laquelle a lieu un transfert d'électron. C'est-à-dire une réaction durant laquelle une espèce chimique dite oxydant reçoit un ou plusieurs électrons d'une autre espèce chimique dite réducteur.
Un oxydant, également appelé agent d'oxydation, correspond à un ion, un corps simple ou un composé qui, lors d'une réaction d'oxydoréduction, reçoit un ou plusieurs électrons d'une autre espèce chimique. Lavoisier mettra en évidence en 1772, suite à ses manipulations du mercure, le rôle du dioxygène dans certaines réactions d'oxydoréduction. D'où le nom oxydation qui signifie "combinaison avec l'oxygène".
Un réducteur, également appelé agent de réduction, correspond à un ion, un corps simple ou un composé qui, lors d'une réaction d'oxydoréduction, cède un ou plusieurs électrons à une autre espèce chimique. Réduction quant à lui signifie "l'extraction d'un métal de son oxyde", une définition connue en métallurgie.
Les réactions d'oxydo-réduction forment une grande famille puisqu'elles comprennent de nombreuses réactions chimiques. En effet, elles interviennent dans les combustions, certains dosages métallurgiques mais également la corrosion des métaux, l'électrochimie et la respiration cellulaire.
Ces réactions sont alors essentielles puisqu'elles jouent un rôle fondamental en biologie : elles permettent la transformation de l'oxygène en eau, de formule H2O, au sein des organismes vivants. Elles sont également massivement utilisées dans l'industrie humaine, notamment afin d'obtenir de la fonte à partir de différents minerais composés d'oxyde de fer grâce à une réduction, puis de fer et d'acier à partir de la fonte grâce à une réaction d'oxydation.
Ces différentes utilisations peuvent être expliquée par l'extrême mobilité de l'électron, sa légèreté mais également son omniprésence dans toutes les formes de la matière.
Les demi-équations
Puisque dans une réaction d'oxydo-réduction, le réducteur s'oxyde, c'est la réaction d'oxydation et l'oxydant se réduit, c'est la réaction de réduction, l'oxydoréduction se compose donc de deux demi-réactions : une oxydation et une réduction.
Elles se présentent sous la forme suivante :
- Oxydation
- réducteur(1) = oxydant(1) + n e-
- Réduction
- oxydant(2) + n e- = réducteur(2)
- Oxydoréduction qui représente donc la "somme" de l'oxydation et de la réduction
- oxydant(2) + réducteur(1) → oxydant(1) + réducteur(2)
Notons que dans les demi-équation, les flèches n'apparaissent que si la réaction est totale, c'est à dire quand K > 10 000
Le potentiel d'oxydo-réduction
Le caractère oxydant ou réducteur d'une espèce dépend de la réaction chimique et des espèces qui interagissent entre elles. En effet, l'élément réducteur dans une réaction peut devenir l'oxydant d'une autre réaction. C'est pour cela que l'on construit une échelle de force oxydante (ou de force réductrice selon le sens donné à cette échelle) afin d'obtenir le potentiel d'oxydo-réduction se mesurant en volt.
En outre, le potentiel d'oxydo-réduction dépend du contexte chimique, notamment du pH, mais aussi du contexte physique puisque les effets de la lumière peuvent intervenir dans la nature comme ce qui est le cas avec la photosynthèse chez les plantes ou la photographie avec l'Homme.
Les réactions acido-basiques

Acide et base selon Brönsted
Un acide est une espèce chimique capable de céder un proton H+.
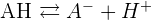
Une base est une espèce chimique capable de capter un proton H+.
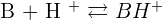
On obtient donc une réaction acido-basique :
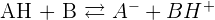
Dans cet exemple, on peut alors parler de :
- Couple AH/A-
- Couple BH+/B
Il y a un transfert d'un proton H+ entre l'acide d'un couple et la base d'un autre couple.
A chaque acide est associé une base qui est dite base conjuguée (réciproquement). Les deux forment un couple Acide/Base.
Le pH
Le pH, ou encore potentiel hydrogène, correspond à une mesure de l'activité chimique de ce qu'on appelle les hydrons dans une solution. Mais vous les connaissez plus certainement sous le nom de protons ou encore ions hydrogènes. De façon plus particulière, ces protons, dans une solution aqueuse, se présent sous la forme de l'ion hydronium qui représente le plus simple des ions oxonium.
Le pH est, le plus souvent, utilisé afin de mesurer l'acidité ou encore la basicité de la solution. On peut alors la déterminer avec l'échelle suivant dans le cas d'un milieu aqueux à 25°C :
- une solution de pH égal à 7 est considérée comme étant neutre ;
- une solution de pH inférieur à 7 est considérée comme étant acide. De ce fait, plus son pH diminue, plus elle est acide ;
- une solution de pH supérieur à 7 est considérée comme étant basique. De ce fait, plus son pH augmente, plus elle est basique.
Mais la définition que nous connaissons aujourd'hui du pH, définition de Sorensen, n'a été officiellement reconnue qu'à partir du milieu du XXe siècle par l'UICPA.
L’UICPA, l’Union Internationale de Chimie Pure et Appliquée est une organisation non gouvernementale ayant son siège à Zurich, en Suisse. Créée en 1919, elle s’intéresse au progrès de la chimie, de la chimie physique et de la biochimie. Ses membres sont les différentes sociétés nationales de chimie et elle est membre du Conseil International pour la Science.
L’UICPA est une autorité reconnue dans le développement des règles à adopter pour la nomenclature, les symboles et autres terminologies des éléments chimiques et leurs dérivés via son Comité Interdivisionnel de la Nomenclature et des Symboles. Ce comité fixe la nomenclature de l’UICPA.
Cette définition est donc celle que nous retrouvons dans les manuels scolaires et s'énonce ainsi :
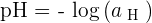
Avec aH, également noté aH+ ou [H+], qui correspond à l'activité des ions hydrogène H+. aH correspond donc à une grandeur sans dimension tout comme le pH.
Néanmoins, cette définition ne nous permet pas d'obtenir des mesures directes du pH ni même des calculs. En effet, le pH dépend uniquement de l'activité des ions hydrogènes. De ce fait, le pH dépend de plusieurs autres facteurs découlant de cette activité. On peut par exemple parler de l'influence du solvant ou encore de la température.
Il reste cependant possible d'obtenir des valeurs approchées du pH en utilisant ce calcul. Pour cela, il est nécessaire de faire appel à des définitions de l'activité.
Cette définition formelle ne permet pas des mesures directes de pH, ni même des calculs. Le fait que le pH dépende de l’activité des ions hydrogène induit que le pH dépend de plusieurs autres facteurs, tels que l’influence du solvant. Toutefois, il est possible d’obtenir des valeurs approchées de pH par le calcul, à l’aide de définitions plus ou moins exactes de l’activité.
Remarque :
le p de pH représente la fonction "- log" donc ici - log (H). Donc si on parle de pOH ou de pKa, cela signifie que l'on parle de - log (OH) et de - log (Ka).
Nouvelle définition du pH
Aujourd'hui, une autre définition du pH a été donné par l'UICPA. Cette définition, déterminée grâce à une méthode électrochimique expérimentale, consiste à utiliser la relation de Nernst dans une cellule électrochimique définie comme qui suit :
Électrode de référence | Solution de KCl concentré | Solution X | H2 | Pt (électrode à hydrogène)
Ainsi, via des mesures de ce qu'on appelle force électromotrice, également notée fem ou f.e.m., de la cellule avec une solution de référence notée S, on peut obtenir la relation suivante : 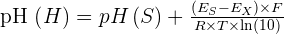
Avec :
- pH(X) représentant le pH de la solution inconnue ;
- pH(S) représentant le pH tabulé de la solution de référence S ;
- EX représentant la f.e.m. de la cellule avec la solution inconnue X ;
- ES représentant la f.e.m. de la cellule avec la solution de référence S à la place de la solution X
- F = 96 485 C mol−1 représentant la constante de Faraday
- R = 8,314 472 J mol−1 représentant la constante universelle des gaz parfaits
- Et T représentant la température absolue, en kelvins
La mesure de pH
La mesure du pH peut se faire à l'aide d'outils comme :
- Le papier pH qui indique la valeur du pH à une unité près ;
- Ou le pHmètre qui indique, quant à lui, une valeur du pH à 0.1 unité près.
A noter que le pH est plus généralement mesuré grâce au pH-mètre, celui-ci reposant sur l'électrochimie et restant plus précis que le papier pH qui n'est qu'un indicateur. Le pH-mètre est appareil composé d'une électrode combinée spéciale, également appelée électrode de verre, ou encore de deux électrodes séparées. De façon générale, l'électrode de référence utilisée dans les pH-mètres correspond à une électrode au calomel saturée, également notée ECS.
Mais le pH peut également être trouvé par calcul :
En effet, d'après la loi de Nernst, 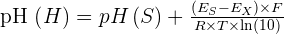
Avec :
- X représentant la solution dont on cherche à déterminer le pH ;
- S représentant la solution de référence ;
- R représentant la constante de gaz parfaits ;
- T représentant la température ;
- F représentant la constante de Faraday.
Il peut être intéressant de noter que, à une température de 298 K, on obtient :
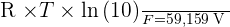










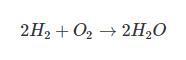












Si vous désirez une aide personnalisée, contactez dès maintenant l’un de nos professeurs !
Bonjour,
Je voudrais solliciter un conseil de votre part.
Je suis allergique à la poudre à lever (= levure chimique = E500 = carbonate acide). L’industrie alimentaire a tendance à en mettre un peu partout et il m’est de plus en plus difficile d’éviter le E500. Je cherche une antidote.
Ma question est : quelle substance pourrait faire une réaction chimique avec du E500 pour le neutraliser. Une substance (par exemple basique) que je pourrais avaler en même temps afin d’éviter de déclencher l’allergie. J’ai déjà questionné des pâtissiers, sans succès, alors je me tourne vers des chimistes c’est mon dernier espoir.
Merci d’avance pour votre réponse, je vous en serai très reconnaissante.
Amicalement,
Chantal
Chantal LANG
Genève, Suisse
chantal@span.ch
Bonjour Prof de chimie,
vos documents sont remarquables.
S’ils contiennent des éléments copiés sur un autre site, assurez vous que vous avez bien l’autorisation de l’auteur pour cette copie. Nous vous rappelons que seules de courtes citations peuvent être reproduites sans autorisation.
L’équipe d’intellego